Accueil > Hepatitis Viruses and Pathobiology of Chronic Liver Diseases > Axe 2: Pathogénie moléculaire des maladies du foie et prédisposition au CHC
Axe 2: Pathogénie moléculaire des maladies du foie et prédisposition au CHC
Contexte
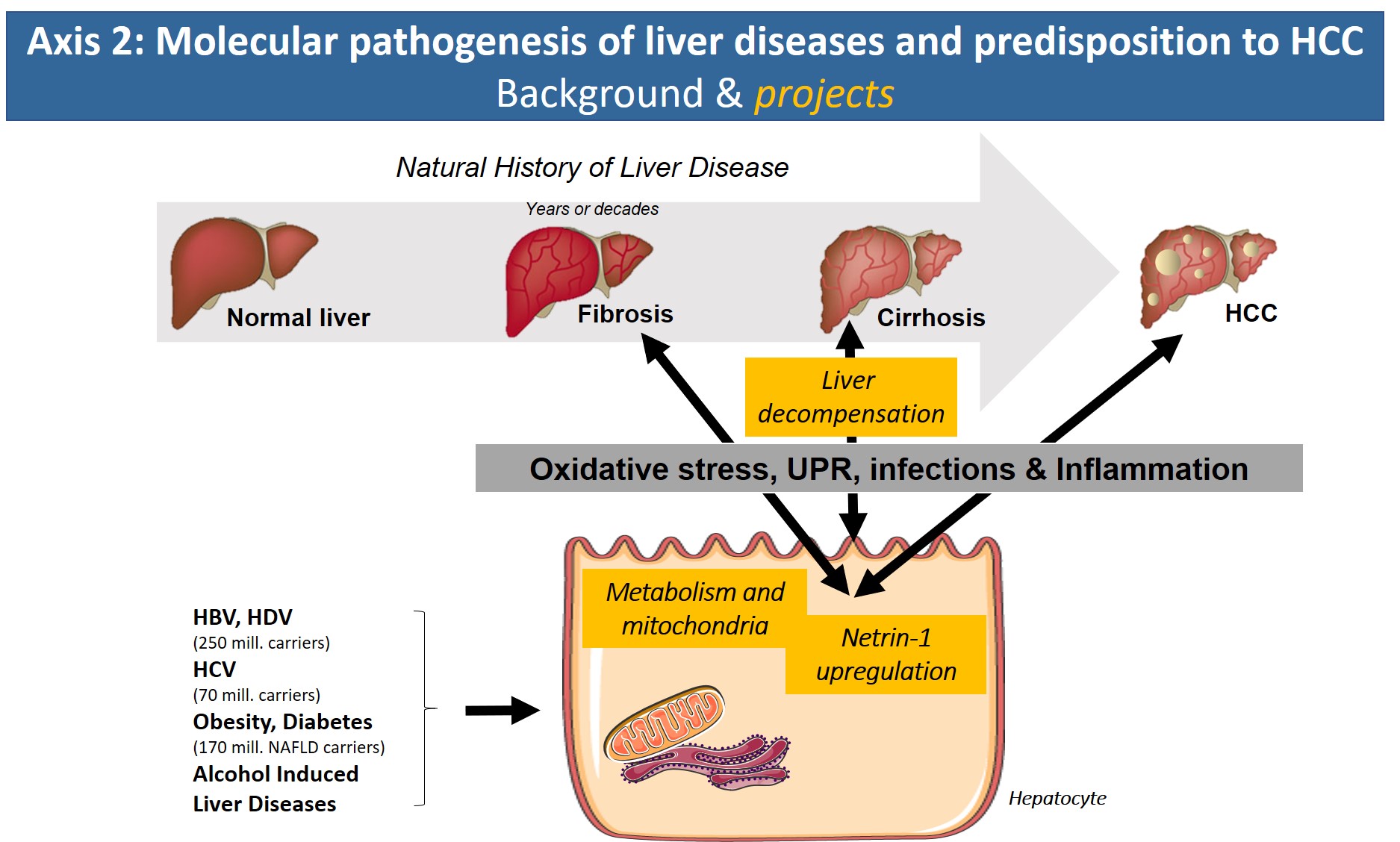
Avec l’arrivée en clinique de nouvelles stratégies de traitement antiviral à action directe qui éliminent efficacement le HCV, réduisent ou permettent une régression de la fibrose hépatique, et diminuent le risque de CHC associé au HCV, l’axe abordera de nouvelles pistes. Sur la base de notre expertise en pathologie moléculaire du HCV, nous avons commencé à rechercher les dénominateurs communs des pathologies qui sous-tendent l’hépatite chronique B/D, la maladie alcoolique du foie et l’obésité/syndrome métabolique (NASH). Dans toutes ces étiologies, il a été démontré que les flux métaboliques altérés, le stress oxydatif, l’inflammation et la signalisation cellulaire remaniée ont un impact sur la progression de la maladie. L’identification de cibles moléculaires communes, de voies de signalisation ou de réactions inflammatoires partagées par ces étiologies aura un impact clinique bénéfique en raison du manque d’options thérapeutiques pour la fibrose hépatique et en particulier la cirrhose et le CHC.
Objectifs
Dans ce contexte, nos objectifs spécifiques seront :
1°) D’identifier le rôle des changements métaboliques et du stress oxydatif induits par le virus dans les maladies hépatiques induites par HCV et HBV/HDV.
2°) D’identifier le rôle de la voie de la netrin-1/UNC5 comme un déclencheur des processus inflammatoires et métaboliques pro-fibrogènes et pro-néoplasiques.
3°) De déchiffrer le rôle de l’inflammation et de la modulation immunitaire dans les maladies du foie en phase terminale et leur contribution aux complications de la cirrhose et aux mauvais résultats (événements septiques, défaillance multi-organique).
Personnel permanent
Bartosch B (DR2), Combet C (CRCN), Lebosse F (PHU), Parent R (CRCN), Grigorov B (MCU), Molle J (AI).
Publications
Lebossé F, Gudd C, Tunc E, Singanayagam A, Nathwani R, Triantafyllou E, Pop O, Kumar N, Mukherjee S, Hou TZ, Quaglia A, Zoulim F, Wendon J, Dhar A, Thursz M, Antoniades CG, Khamri W. CD8+ T cells from patients with cirrhosis display a phenotype that may contribute to cirrhosis-associated immune dysfunction. EBioMedicine. 2019 Nov;49:258-268.
Bassot A, Chauvin MA, Bendridi N, Ji-Cao J, Vial G, Monnier L, Bartosch B, Alves A, Cottet-Rousselle C, Gouriou Y, Rieusset J, Morio B. Regulation of Mitochondria-Associated Membranes (MAMs) by NO/sGC/PKG Participates in the Control of Hepatic Insulin Response. Cells. 2019 Oct 25;8(11):1319. doi: 10.3390/cells8111319.
Lévy PL, Duponchel S, Eischeid H, Molle J, Michelet M, Diserens G, Vermathen M, Vermathen P, Dufour JF, Dienes HP, Steffen HM, Odenthal M, Zoulim F, Bartosch B. Hepatitis C virus infection triggers a tumor-like glutamine metabolism. Hepatology. 2017 Mar;65(3):789-803.
Lahlali T, Plissonnier ML, Romero-López C, Michelet M, Ducarouge B, Berzal-Herranz A, Zoulim F, Mehlen P, Parent R. Netrin-1 Protects Hepatocytes Against Cell Death Through Sustained Translation During the Unfolded Protein Response. Cell Mol Gastroenterol Hepatol. 2016 Jan 9;2(3):281-301.e9.
Plissonnier ML, Lahlali T, Michelet M, Lebossé F, Cottarel J, Beer M, Neveu G, Durantel D, Bartosch B, Accardi R, Clément S, Paradisi A, Devouassoux-Shisheboran M, Einav S, Mehlen P, Zoulim F, Parent R. Epidermal Growth Factor Receptor-Dependent Mutual Amplification between Netrin-1 and the Hepatitis C Virus. PLoS Biol. 2016 Mar 31;14(3):e1002421.